前言:
今日(8月17日)上午,因有感于某自媒体撰写的一篇有关“阿齐沙坦片”的文章,小编撰写了“闲聊 II 因“阿齐沙坦片(化3类)”获批引发的“遐思”,并在自媒体“药迅社”进行了发表。之所以选择在“药迅社”发表,是因为,药迅社的关注群体基本都是RA,多数RA可能在昨晚(8月16日)在其朋友圈都看到了闺蜜甲转给小编的有关“阿齐沙坦片”的那篇推断百奥药业未做临床试验,亦或BE试验的文章。“闲聊 II 因“阿齐沙坦片(化3类)”获批引发的“遐思”一发表,部分圈友基本都看明白了,但是也有部分圈友给小编在朋友圈留言,没看明白,或者没看懂文章末尾“。这与当年上海安必生与杭州民生就“孟鲁司特钠咀嚼片”的关联一样”这句话。为了让圈友更为清晰地了解某些化药3类开发过程(重点关注验证性临床试验是否开展)及MAH制度试点及正式落地后,某些药物的申请人在上市申请阶段与临床申请时不一致等现象,小编以北京百奥药业的阿齐沙坦片为例,简单总结如下:北京百奥药业的阿齐沙坦片从立项到获批历时10多年,2013年由其合作方“河北仁合益康药业有限公司”按照原化药3.1类递交临床试验申请(见图1)”,并于2017年获得临批,同年开展其III期临床试验(以奥美沙坦酯片(傲坦)为对照,评价北京百奥药业有限责任公司提供的阿齐沙坦片治疗轻、中度原发性高血压的有效性和安全性。)(见图2),并分别在2017年、2019年进行2个规格(40mg、20mg)的BE试验(见图3、4)。注:前些年的审评积压,导致多数品种在临床试验申请阶段,历时3-5年,实属正常。原化药3.1是指已在国外上市销售的制剂及其原料药,和/或改变该制剂的剂型,但不改变给药途径的制剂。
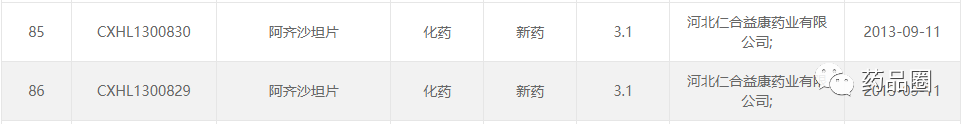
图1
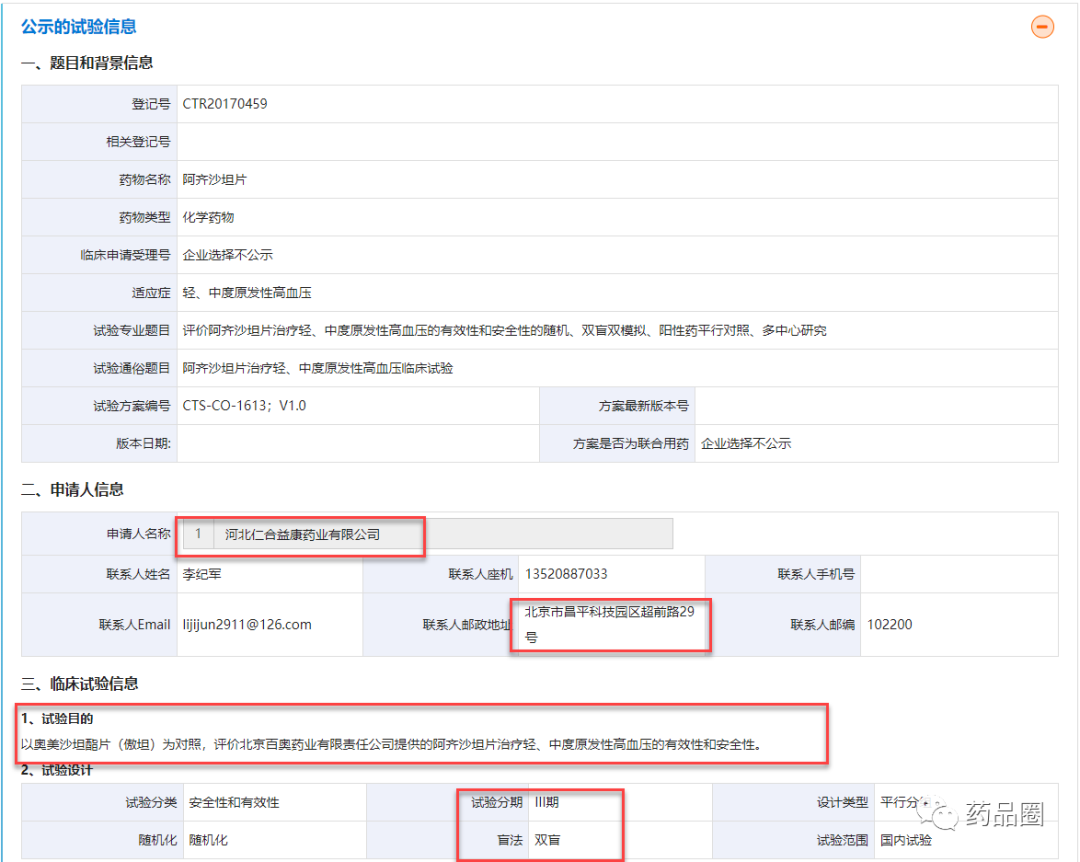
图2
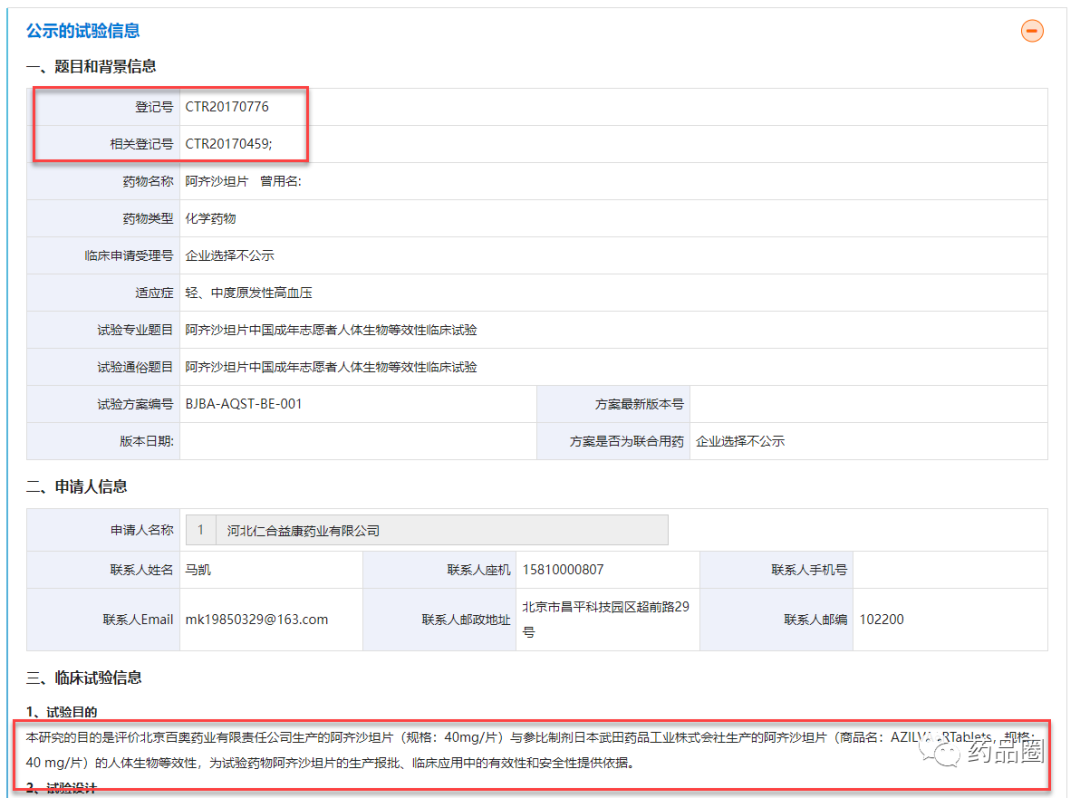
图3
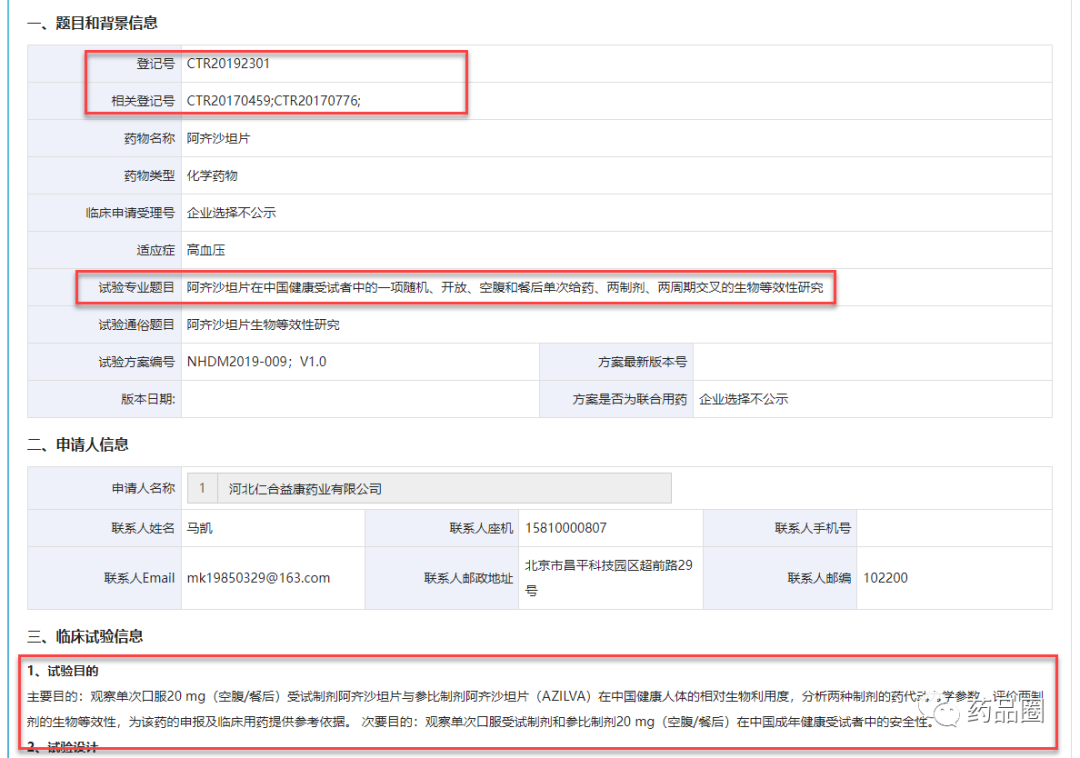
图4
通过上面的分析及截图,相信圈友们一定懂得了“百奥药业一定与其他申请人进行了关联!”。但不了解近年药品监管领域相关法律法规改革,尤其是MAH制度与国际接轨的圈友,可能对百奥药业为啥与其他企业关联有所困惑?
请随小编简单回顾一下安必生的孟鲁司特钠咀嚼片的案例,您就会懂了。
在MAH制度试点之前,申请药物临床试验或者上市申请的申请人只能是药品生产企业。2015年以来我国药监法规有关MAH的制度与国际接轨,上海安必生成为国内第一家药品研发机构可以拥有药品批准文号,成为药品上市许可持有人(MAH)。2015年年4月,上海安必生的合作方杭州民生滨江制药有限公司递交了“孟鲁司特钠咀嚼片”的上市申请(见图5),审评期间,随着MAH的制度的落地,申请人变更为安必生(见图6)。注:安必生的“孟鲁司特钠咀嚼片”获批后,通过补充申请增加了另外一个生产厂商 青岛百洋制药有限公司。
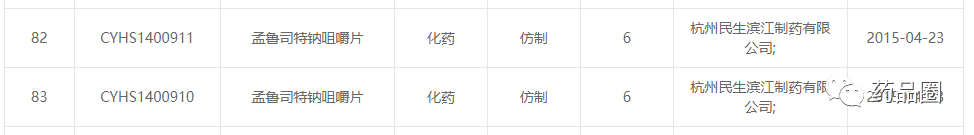
图5
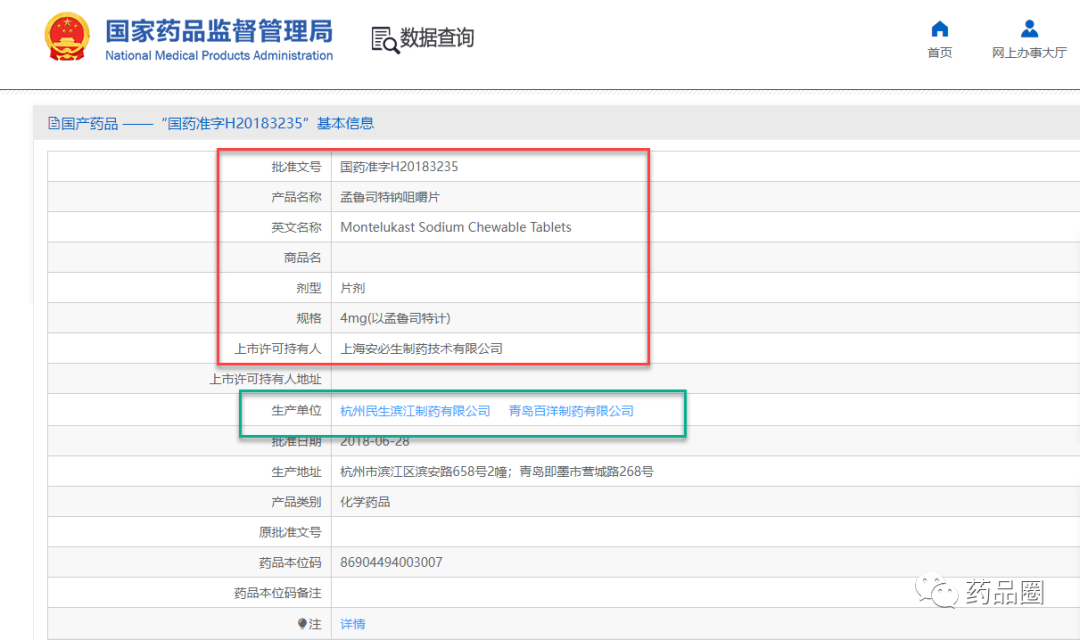
图6
看到上面的分析与截图,相信从事RA的圈友们,基本就知道个大概了,百奥药业与“河北仁合益康药业有限公司”进行的关联。这与当年上海安必生与杭州民生就“孟鲁司特钠咀嚼片”的关联一样。
还是那句老话,化学仿制药,尤其是化3类的开发,具体品种具体分析,没有什么捷径可走!


